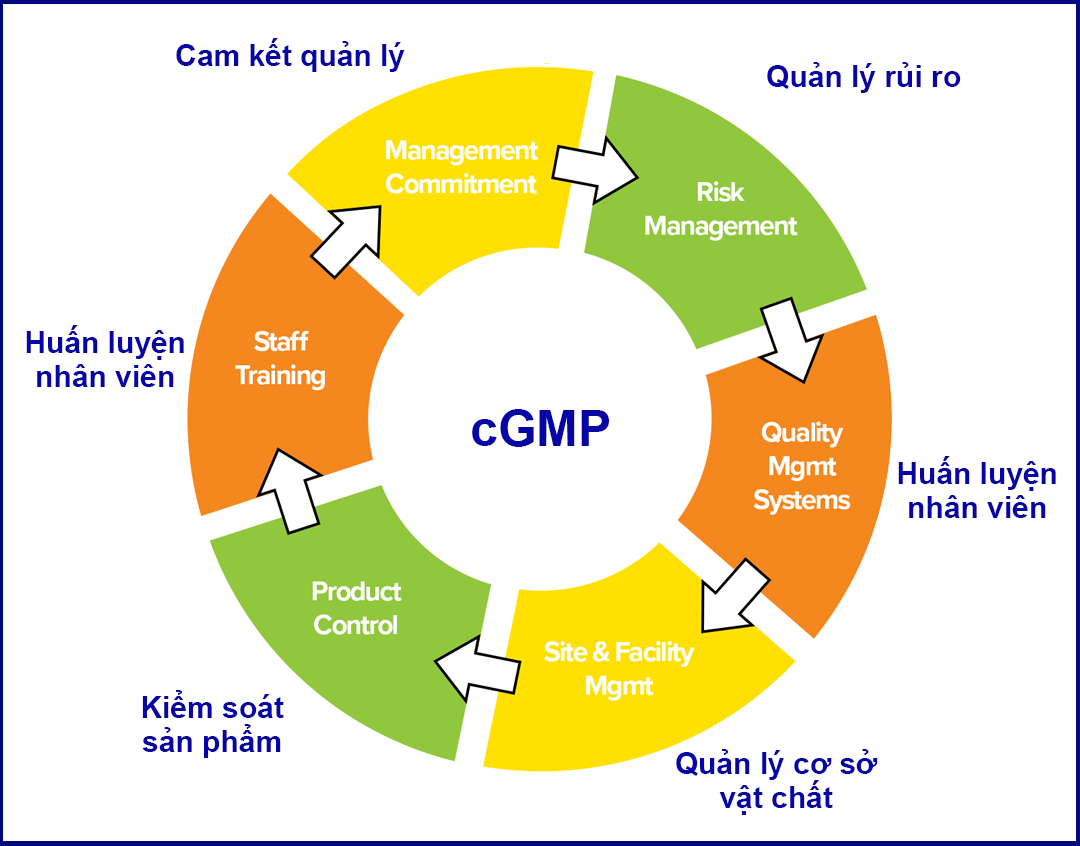
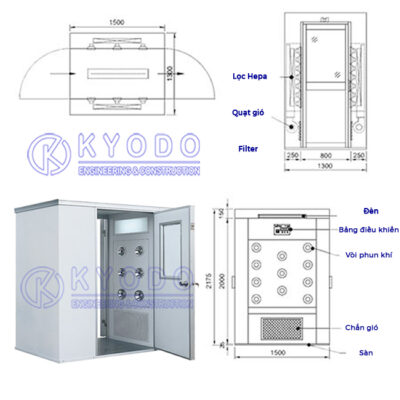
Trong lĩnh vực sản xuất Dược và Mỹ phẩm, từ đầu chúng ta thường nghe đến tiêu chuẩn cGMP, thế nhưng đa số mọi người chưa biết đến thực tế có 2 tiêu chuẩn cùng tên “cGMP”. Theo dõi nội dung sau của KYODO để biết thêm về cGMP là gì? Phân biệt CGMP ASEAN và FDA (USA), ý nghĩa và tầm ảnh hưởng của 2 tiêu chuẩn này với các nhà máy sản xuất dược phẩm, mỹ phẩm và trong các lĩnh vực sản xuất khác.
I. Tiêu chuẩn cGMP ASEAN (Cosmetic Good manufacturing Practices Asean)
1. cGMP ASEAN là gì?
Tại các nước Đông Nam Á (bao gồm Việt Nam), thực hành tốt sản xuất Mỹ phẩm (CGMP ASEAN) là những nguyên tắc yêu cầu nhằm đáp ứng về điều kiện sản xuất dành riêng cho mỹ phẩm.
Các quy tắc này được quy định tại hướng dẫn của ASEAN về Thực hành tốt Sản Xuất Mỹ Phẩm (ASEAN Guidelines For Cosmetic Good Manufacturing Practice) được quy đinh bởi “Hiệp định về hệ thống hòa hợp ASEAN trong quản lý mỹ phẩm” do Uỷ ban Mỹ phẩm ASEAN (ASEAN Cosmetic Committee) chịu trách nhiệm thực hiện.

Ở Việt Nam, Cục Quản lý dược – Bộ Y tế có trách nhiệm xem xét hồ sơ, đánh giá và cấp Giấy chứng nhận cơ sở đáp ứng các nguyên tắc, tiêu chuẩn “Thực hành tốt sản xuất mỹ phẩm“ theo quy định tại Thông tư 06/2011/TT-BYT.
Theo Bộ Y Tế Việt Nam, các nhà máy sản xuất mỹ phẩm đều phải đáp ứng đủ tiêu chuẩn CGMP, và có giấy chứng nhận để đảm bảo chất lượng vệ sinh và an toàn thực phẩm.
2. Các yêu cầu khi đánh giá tính an toàn của sản phẩm mỹ phẩm
Các tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường phải đảm bảo các sản phẩm của mình không có hại đối với sức khoẻ con người khi được dùng trong những điều kiện bình thường hoặc những điều kiện thích hợp được hướng dẫn, phù hợp với dạng bào chế, thông tin ghi trên nhãn, hướng dẫn sử dụng, thận trọng đặc biệt, cũng như các thông tin khác cung cấp bởi nhà sản xuất hoặc chủ sở hữu sản phẩm.
Nhà sản xuất, chủ sở hữu sản phẩm phải đánh giá tính an toàn trên mỗi sản phẩm mỹ phẩm theo “Hướng dẫn đánh giá tính an toàn mỹ phẩm của ASEAN“. Giới hạn kim loại nặng và vi sinh vật trong mỹ phẩm phải đáp ứng yêu cầu của ASEAN.
3. Giấy chứng nhận đạt tiêu chuẩn cGMP Asean có hiệu lực trong bao lâu?
Cơ sở đáp ứng các nguyên tắc, tiêu chuẩn CGMP ASEAN được cấp Giấy chứng nhận (trong đó nêu rõ loại dây chuyền sản xuất). Giấy chứng nhận cơ sở đáp ứng các nguyên tắc, tiêu chuẩn cGMP-ASEAN có giá trị 03 năm.
Theo Dự thảo, việc kiểm tra, thanh tra được thực hiện theo 2 hình thức:
- Kiểm tra, thanh tra định kỳ: Kiểm tra, thanh tra định kỳ sẽ được cơ quan quản lý nhà nước có thẩm quyền thông báo trước cho đơn vị được kiểm tra để đơn vị chuẩn bị về việc kiểm tra, thanh tra trước khi tiến hành hoạt động kiểm tra, thanh tra.
- Kiểm tra, thanh tra đột xuất: Kiểm tra, thanh tra đột xuất khi phát hiện cơ sở có dấu hiệu vi phạm nghiêm trọng, không tuân thủ quy định về điều kiện sản xuất mỹ phẩm hoặc do các khiếu nại của khách hàng. Trong trường hợp Kiểm tra, thanh tra đột xuất, cơ quan quản lý nhà nước có thẩm quyền có quyền kiểm tra, thanh tra không cần báo trước.
4. Hình thức xử lý với các cơ sở, nhà máy sản xuất không đáp ứng
- Phải báo cáo khắc phục tồn tại, nộp hồ sơ đăng ký và được cơ quan có thẩm quyền xác nhận hoặc giấy chứng nhận cơ sở đủ điều kiện sản xuất mỹ phẩm.
- Thu hồi các sản phẩm không đáp ứng được chất lượng và điều kiện sản xuất theo quyết định ban hành của Pháp luật.
- Thông báo thu hồi tất cả những sản phẩm kém chất lượng, vi phạm điều kiện sản xuất mỹ phẩm tiêu chuẩn.
- Thanh kiểm tra về thiết bị máy móc, nguyên liệu, quy trình sản xuất, vệ sinh môi trường, vệ sinh nhà máy, nhân viên đến các mẫu thử, tài liệu, chất lượng sản phẩm để kiểm tra khiếu nại của khách hàng.
5. Hồ sơ, thủ tục cấp Giấy chứng nhận
Đơn vị sản xuất có nhu cầu cấp Giấy chứng nhận cơ sở đáp ứng các nguyên tắc, tiêu chuẩn “Thực hành tốt sản xuất mỹ phẩm” của Hiệp hội các nước Đông Nam Á (cGMP ASEAN) để phục vụ cho xuất khẩu gửi hồ sơ đăng ký kiểm tra về Cục Quản lý dược – Bộ Y tế.
Chứng nhận CGMP là một sự đảm bảo về quá trình sản xuất của doanh nghiệp, mang đến những sản phẩm chất lượng, an toàn, tốt nhất khi đưa ra thị trường.
Hồ sơ bao gồm:
- Phiếu đăng ký kiểm tra “Thực hành tốt sản xuất mỹ phẩm”.
- Bản sao Giấy đăng ký kinh doanh hoặc Giấy phép đầu tư.
- Sơ đồ tổ chức và nhân sự của cơ sở (sơ đồ tổ chức phải thể hiện rõ tên, chức danh, trình độ chuyên môn kỹ thuật của các cán bộ phụ trách các bộ phận), quá trình công tác và kinh nghiệm trong lĩnh vực được phân công của các cán bộ phụ trách các bộ phận (sản xuất, kiểm tra chất lượng, đảm bảo chất lượng, nhà kho).
- Chương trình tập huấn, đánh giá kết quả tập huấn “Thực hành tốt sản xuất mỹ phẩm” tại đơn vị.
- Sơ đồ vị trí và thiết kế của nhà máy (bao gồm: sơ đồ mặt bằng tổng thể; sơ đồ đường đi của công nhân; sơ đồ đường đi của nguyên liệu, bao bì, bán thành phẩm, thành phẩm; sơ đồ hệ thống xử lý chất thải).
- Danh mục thiết bị hiện có của nhà máy (bao gồm thiết bị sản xuất và thiết bị kiểm tra chất lượng mỹ phẩm) phải thể hiện được tên thiết bị, năm sản xuất, nước sản xuất và tình trạng của thiết bị.
- Danh mục các mặt hàng đang sản xuất hoặc dự kiến sản xuất (ghi rõ dạng sản phẩm).
- Biên bản tự thanh tra “Thực hành tốt sản xuất mỹ phẩm” (Biên bản tự thanh tra phải thể hiện rõ thời gian thanh tra, thành phần đoàn tự thanh tra, mục tiêu tự thanh tra, kết quả tự thanh tra và các đề xuất thời gian và biện pháp khắc phục các tồn tại).
II. Tiêu chuẩn cGMP USA – current Good manufacturing Practices
cGMP (Current Good manufacturing Practices) – Tạm dịch là thực hành tốt sản xuất hiện hành. Đề cập đến các quy định sản xuất dược phẩm hiện hành được xác nhận bởi FDA – Cục quản lý thực phẩm và dược phẩm Hoa Kỳ (Food and Drug Administration).
1. CGMP FDA áp dụng cho các ngành sản xuất nào?
- Dược phẩm
- Thực phẩm
- Mỹ phẩm
- Thức ăn chăn nuôi
- Thuốc thú y
- Thực phẩm chức năng
- Vắc-xin
- Sản xuất hóa chất
- Sản xuất thiết bị y tế
- Sản xuất dụng cụ y tế
2. Tiêu chuẩn cGMP USA quy định những gì?
Tiêu chuẩn cGMP USA cung cấp cho các hệ thống đảm bảo thiết kế hợp lý, giám sát và kiểm soát tất cả các quá trình sản xuất và các phương tiện sản xuất. Tuân thủ các quy định cGMP để đảm bảo các tiêu chí hàng đầu về chất lượng sản phẩm. Có thể liệt kê cụ thể như: Thiết lập ban đầu về hệ thống quản lý chất lượng, xây dựng cơ sở vật chất đáp ứng, nguyên liệu đầu vào, toàn bộ quy trình vận hành, phát hiện bất thường và sai lệch sản phẩm, duy trì hệ thống thí nghiệm – thử nghiệm đáng tin cậy, …
3. Yêu cầu của tiêu chuẩn thực hành tốt sản xuất cGMP USA
- Có đội ngũ nhân lực và trình độ học vấn chuyên môn tương đối, có phẩm chất và chuẩn mực trong công việc. Có kế hoạch đào tạo, rèn luyện, huấn luyện nghiệp vụ để nâng cao, cập nhật kiến thức và chuyên môn thường xuyên.
- Máy móc, thiết bị, cơ sở vật chất hiện đại, được kiểm định chặt chẽ và định kỳ để đảm bảo chất lượng.
- Các thành phần, nguyên liệu đầu vào được kiểm chứng trước khi sản xuất.
- Kiểm tra, thẩm định rõ ràng các thành phần hóa học, có nguồn gốc xuất xứ rõ ràng, chứng nhận an toàn cho người tiêu dùng.
- Môi trường sản xuất khép kín, đảm bảo vệ sinh và được kiểm soát nghiêm ngặt bằng các dụng cụ, thiết bị và phương tiện hiện đại.

Làm cách nào để FDA có thể xác định một doanh nghiệp, nhà máy sản xuất tuân thủ các quy định theo cGMP?
- FDA kiểm tra cơ sở sản xuất chế biến trên toàn thế giới, bao gồm tất cả các cơ sở vật chất sản xuất nguyên liệu, hoạt chất và thành phẩm.
- FDA dựa vào các báo cáo về các sản phẩm thuốc đã được công bố.
4. Tầm quan trọng của các tiêu chuẩn cGMP USA trong nhà máy sản xuất thuốc – Dược phẩm
Hiện nay, có rất nhiều loại dược phẩm, thực phẩm chức năng, mỹ phẩm khác nhau trên thị trường. Nhưng tình trạng hàng giả, hàng nhái, hàng kém chất lượng đang rất phổ biến. Mà nhu cầu tiếp cận các loại sản phẩm như trên của người tiêu dùng đang tăng cao. Hơn nữa, sự bùng phát của đại dịch Covid mà mỗi chúng ta đều sẽ quan tâm hơn nữa về sức khỏe của bản thân và gia đình. Vì vậy tiêu chuẩn cGMP nói riêng và các tiêu chuẩn khác nói chung như: PIC/S, GMP EU, Japan GMP,… Đóng một vai trò rất quan trọng, giúp người tiêu dùng đánh giá và có một thước đo uy tín để lựa chọn sản phẩm an toàn, hiệu quả.
III. Ý nghĩa và ảnh hưởng của cGMP đến chất lượng sản phẩm
Hiện nay, có rất nhiều loại dược phẩm, thực phẩm chức năng, dược mỹ phẩm khác nhau trên thị trường. Tình trạng hàng giả, hàng không rõ xuất xứ, hàng kém chất lượng đang trôi nổi và rất phổ biến. Vì thế, cả 2 tiêu chuẩn cGMP này đều là một sự đảm bảo về quá trình sản xuất của nhà máy đồng thời mang đến những cam kết về chất lượng sản phẩm. Tóm lại, cả hai tiêu chuẩn cGMP này mang lại các lợi ích như sau:
- Tiêu chuẩn hóa điều kiện vệ sinh và hoạt động kiểm soát vệ sinh nhà xưởng, con người, sản xuất.
- Tạo điều kiện thuận lợi cho việc triển khai HACCP, ISO 22000, GMP (nếu cần).
- Giảm phần lớn nguy cơ ngộ độc, khiếu nại, phàn nàn của khách hàng nhờ ứng dụng cgmp, mang đến các sản phẩm an toàn với người tiêu dùng, đúng công dụng.
- Tăng cường sự uy tín, sự tin cậy, sự hài lòng của nhà phân phối và khách hàng. Khẳng định chất lượng, nâng cao uy tín, tạo dựng niềm tin, thương hiệu cho doanh nghiệp, nhà máy.
- Cải thiện hoạt động tổng thể của doanh nghiệp, tăng cường nhận thức GMP cho nhân sự, tạo dựng môi trường làm việc chuyên nghiệp cho nhân viên.
- Đáp ứng các điều kiện xuất khẩu sản phẩm đến các nước phát triển như Nhật Bản, Mỹ, các nước Châu âu,…

IV. Sự phổ biến của cGMP USA và cGMP ASEAN hiện nay
Tại khu vực Đông Nam Á, cGMP USA đang được ứng dụng ít hơn so với các tiêu chuẩn dược khác. Do nhiều yêu cầu về máy móc thiết bị, quy trình, công nghệ tân tiến và hiện đại. Bắt buộc các doanh nghiệp phải có chi phí đầu tư ban đầu rất lớn. Bên cạnh đó, cách thức xét duyệt, kiểm soát của tiêu chuẩn này yêu cầu cao, chi tiết và tốn nhiều thời gian hơn. Hiện nay chỉ có một vài thành phố ở Mỹ và châu Âu có các cơ sở đạt chứng nhận cGMP USA. Tuy vậy, chất lượng sản phẩm từ các cơ sở đạt chuẩn này đáng tin cậy hơn nhiều.
Ngược lại, ở khu Việt Nam và các nước lân cận, cGMP ASEAN là yêu cầu chung đặc biệt quan trọng. Giúp doanh nghiệp cung cấp các sản phẩm mỹ phẩm qua thị trường các nước trong khu vực để tiêu thụ. Vì vậy, chứng nhận cGMP ASEAN rất thiết thực, có tính phổ biến và dễ dàng đạt được hơn so với tiêu chuẩn của Mỹ.
Hi vọng qua nội dung này quý vị độc giả đã khám phá ra được cGMP là gì? Và nên ứng dụng tiêu chuẩn nào cho cơ sở sản xuất của mình, cảm ơn đã theo dõi.
Xem thêm: Tiêu chuẩn phòng sạch GMP